Nomenclatura dei dispositivi medici: EMDN, GMDN, UMDNS, CND

Per nomenclatura dei dispositivi medici si intende un sistema specifico di codifica e denominazione il cui obiettivo è facilitare la classificazione e l'identificazione di tutti i dispositivi medici disponibili sul mercato. Sfortunatamente, l'obiettivo di stabilire un sistema standardizzato a livello mondiale per migliorare la gestione e la trasmissione delle informazioni sui dispositivi medici è lontano dall'essere raggiunto. Molti hanno tentato di implementare un sistema armonizzato; tuttavia, ciò ha portato solo a innumerevoli abbreviazioni e codici confusi per vari scopi.
Ci sono Paesi che non hanno alcun sistema di nomenclatura e basano le loro procedure regolamentari, acquisizioni, operazioni doganali, mantenimento delle scorte e manutenzione dei dispositivi medici sul loro sistema nazionale (o su nessun sistema).
Sai quanti sistemi di nomenclatura diversi esistono? Ecco alcuni esempi GMDN, UMDNS, CND, GPC, SNOMED CT, EMDN, MCN, UNSPSC, CIE... e molti altri (senza contare i sistemi sviluppati a livello nazionale).
Índice de contenidos
Index of contents
Index du contenu
Inhaltsverzeichnis
Indice dei contenuti
- Per l'amor di Dio, facciamo chiarezza in questo caos di nomenclature!
- Sistema universale di nomenclatura dei dispositivi medici (UMDNS)
- Nomenclatura Mondiale dei Dispositivi Medici (GMDN)
- Classificazione Nazionale dei Dispositivi Medici in Italia (CND)
- Nomenclatura Europea dei Dispositivi Medici (EMDN)
1. Per l'amor di Dio, facciamo chiarezza in questo caos di nomenclature!
Ecco un riassunto dei sistemi di nomenclatura più comuni. La coesistenza di diverse nomenclature rende più difficile garantire una copertura sanitaria universale.
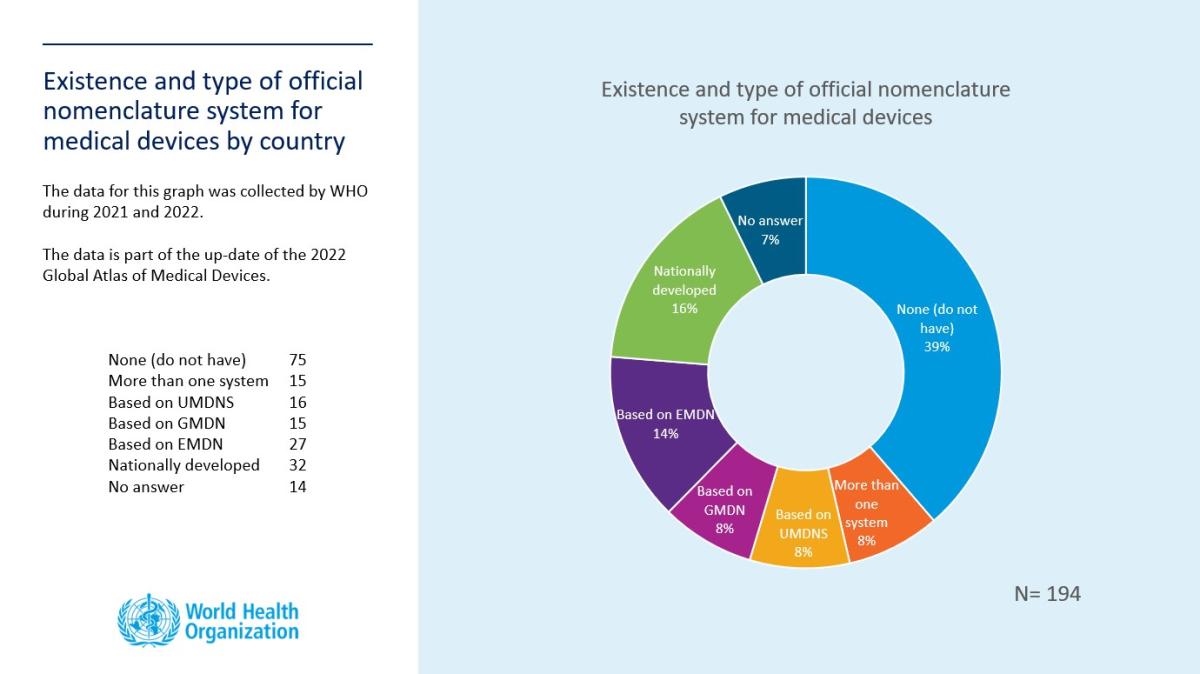
Fonte: Atlante mondiale dei dispositivi medici 2022, OMS (in inglese)
2. Sistema universale di nomenclatura dei dispositivi medici (UMDNS)
Il Sistema Universale di Nomenclatura dei Dispositivi Medici, come suggerisce il nome, segue un approccio universale ed è stato sviluppato dall'organizzazione non governativa e senza scopo di lucro Emergency Care Research Institute (ECRI).
2.1 Riassunto:
- Sistema poligerarchico
- Codici a cinque cifre per i nomi
- Codici associati alla definizione e descrizione dell'uso previsto
Tutti gli utenti devono abbonarsi per visualizzare la gerarchia, la struttura e le relazioni tra i termini. È possibile che molti utenti debbano acquistare altri prodotti dell'ECRI per avere pieno accesso ai vari tipi di licenza. A differenza del sistema GMDN, l'UMDNS non è richiesto ufficialmente in nessun Paese del mondo, ma spesso viene utilizzato per basare o adattare nomenclature sviluppate a livello nazionale (ad esempio, in Iran o Iraq).
3. Nomenclatura Mondiale dei Dispositivi Medici (GMDN)
Per molto tempo, la Nomenclatura Mondiale dei Dispositivi Medici sembrava essere una possibile soluzione universalmente utile per i sistemi di nomenclatura. La GMDN è stata sviluppata dal Comitato Europeo di Normalizzazione e da esperti di dispositivi medici ed è gestita dall'Agenzia GMDN.
3.1 Riassunto:
- Sistema poligerarchico
- Identificazione del prodotto tramite numeri unici a cinque cifre e termine associato
- Definizione con gli scopi previsti
- Categorie di prodotti
Quest’impresa senza scopo di lucro genera entrate tramite la vendita di codici GMDN per riuscire ad aggiornare costantemente i dati. Ciò significa che la nomenclatura GMDN non è gratuita per i produttori o per chi la consulta e richiede inoltre un'iscrizione.
In Australia, il sistema GMDN è imposto per legge; altri Paesi utilizzano invece sistemi misti o combinati. Ad esempio, in Francia il sistema GMDN è utilizzato per l'acquisizione e la commercializzazione, mentre il nuovo EMDN è stato implementato per scopi come la regolamentazione, la registrazione o la sorveglianza. Altri paesi, come la Polonia, hanno incorporato la GMDN nella loro legislazione, ma permettono anche l'uso di altre nomenclature, il che include l'applicazione aggiuntiva dell'EMDN.
4. Classificazione Nazionale dei Dispositivi Medici in Italia (CND)
La CND è stata sviluppata dalle autorità italiane. Il codice GMDN era la chiave di registrazione obbligatoria in Italia in precedenza, ma a causa della difficoltà di utilizzo e della mancanza di disponibilità, il GMDN è stato eliminato su richiesta dei produttori di dispositivi medici. Di conseguenza, la CND è stata creata mappando i due sistemi di nomenclatura dal 2007 e facilitando quindi l'accesso e l'uso.
Alla luce del regolamento MDR e IVDR, l'UE ha deciso di adottare il sistema CND italiano come base per sviluppare la nuova Nomenclatura Medica Europea (EMDN) che viene utilizzata per la registrazione e la regolamentazione dei dispositivi medici in EUDAMED. Nel 2020, la Commissione Europea e il Comitato Tecnico italiano hanno annunciato l'ingresso aggiornato e il pieno allineamento della GMDN con la CND. Si tratta di una pietra miliare e di una sfida per i 27 Paesi dell'Unione Europea.
5. Nomenclatura Europea dei Dispositivi Medici (EMDN)

L'Unione Europea ha stabilito nuovi requisiti per un sistema comune di nomenclatura in conformità con l'Articolo 26 del Regolamento 2017/745 sui dispositivi medici (MDR) e l'articolo 23 del Regolamento 2017/745 sui dispositivi medici per diagnosi in vitro (IVDR). L'obiettivo è supportare il database europeo sui dispositivi medici (EUDAMED) e viene utilizzato a scopi regolamentari nei 27 Stati membri dell'UE per soddisfare tutti i nuovi requisiti stabiliti.
5.1 Riassunto:
- Gerarchia di sette livelli
- Struttura alfanumerica
- Tre livelli principali per i dispositivi medici: Categoria, Gruppi, Tipi
Come già detto, l'EMDN viene applicato dai 27 paesi dell'UE, che costituiscono il 14% dei Paesi del mondo.
5.2 Principali obiettivi dell'EMDN:
- Trasparenza
- Accessibilità
- Disponibilità
- Inclusione
- Prevedibilità
- Riconoscimento internazionale
La nomenclatura dell'EMDN è gratuita, e i termini, le descrizioni e i codici sono completamente accessibili a tutti gli utenti.
Il foglio informativo dell’European Migration Network, Commissione Europea 25/05/2021, afferma:
«Nessun produttore o persona fisica o giuridica deve essere soggetto a una tassa né subire discriminazioni di alcun tipo, rispetto ad altri operatori, in relazione all'uso della nomenclatura».
I codici EMDN sono obbligatori, così come l'inclusione delle informazioni EMDN nel fascicolo tecnico del dispositivo medico e nella dichiarazione di conformità. Come puoi vedere, la terminologia della nomenclatura EMDN è cruciale per registrare e vendere qualsiasi tipo di dispositivo medico nell'Unione Europea. Per questo è rilevante scegliere fornitori di servizi di traduzione aggiornati e specializzati in dispositivi medici, capaci di fornire traduzioni che rispettino i requisiti normativi.
Come indicato in quest’articolo, esistono numerose nomenclature utilizzate in tutto il mondo per diversi scopi. Tuttavia, grazie all'approccio dell'UE ci stiamo avvicinando sempre di più all'armonizzazione del quadro normativo e al raggiungimento di una copertura sanitaria universale. Metà dei Paesi del mondo non ha ancora implementato alcun sistema di nomenclatura, ma seguendo i principi dell'EMDN, sono sicura che presto molti lo incorporeranno nelle loro legislazioni. La standardizzazione è importante e parlare la stessa lingua quando si tratta di dispositivi medici è essenziale per rafforzare i sistemi sanitari a livello globale.
Forse potrebbero interessarti anche questi altri blog:

Alejandra Keller è madrelingua tedesca e spagnola, con un’elevata padronanza della lingua inglese. È laureata in Traduzione presso l’Università di Heidelberg e ha vissuto e studiato in Germania, negli Stati Uniti, in Irlanda, in Spagna e in Perù. Animata da una forte passione per la comunicazione internazionale, attualmente lavora come Project Manager presso AbroadLink.



Aggiungi un commento